Categoría: Investigación Científica y Tecnológica
Artículo original
Aproximación a la determinación de la estructura tridimensaional de la proteína fibra del virus oncolítico Ad5-Δ24-RGD mediante modelamiento por homología
Federico Matheus Navarro1 y Mauricio Pulido Jiménez 2
1.Estudiante 11º grado, Gimnasio Campestre. 2. Director CEBM, Gimnasio Campestre.
Correspondencia para el autor: centrobiomol@campestre.edu.co
Recibido: 19 de abril de 2022
Aceptado: 25 de mayo de 2022

Resumen
Mediante el uso de modelamiento por homología se determinó la estructura tridimensional de la proteína fibra del adenovirus oncolítico modificado Ad5-Δ24-RGD. La inserción del motivo RGD en cada uno de los tres monómeros que constituyen a la proteína fibra condujo a la aparición de una región que mostró dos segmentos con estructura de hebra beta dispuestos en sentido antiparalelo. Dichos segmentos están ligados entre sí por secciones de tipo giro beta. La comparación de las estructuras espaciales de la proteína nativa y la modificada por la inserción del motivo RGD reveló variaciones conformacionales significativas que podrían ser la explicación de los cambios en la capacidad infectiva del adenovirus modificado que se han reportado en estudios anteriores.
Palabras claves: Adenovirus, proteína fibra, modelamiento por homología, hebra beta, motivo RGD.
Using homology modeling, the three-dimensional structure of the fiber protein of the modified oncolytic adenovirus Ad5-Δ24-RGD was determined. Insertion of the RGD motif into each of the three monomers constituting the fiber protein led to the appearance of a region showing two beta-stranded segments arranged in an antiparallel direction. These segments are linked together by beta-turn-type sections. Comparison of the spatial structures of the native protein and the one modified by the insertion of the RGD motif revealed significant conformational variations that could be the explanation for the changes in the infective capacity of the modified adenovirus reported in previous studies.
Key words: Adenovirus, fiber protein, homology modeling, beta-strand, RGD motif.

Imagen de: “Esquema de un virus CMV” por Emmanuel Boutet
«Los adenovirus hacen parte de una familia de virus altamente contagiosos y que comúnmente atacan las mucosas de los sistemas respiratorio y nervioso, los ojos, los intestinos y las vías urinarias.«

Imagen del Instituto Nacional del Cáncer

Imagen del Instituto Nacional del Cáncer
Introducción
El cáncer es una patología provocada por la proliferación incontrolada de las células que constituyen los tejidos de los seres vivos. Este aumento en el número de células conduce a la aparición de tumores que pueden provocar modificaciones estructurales y funcionales del órgano en el que se encuentran (Jones & Baylin, 2007). En ocasiones las células tumorales pueden desprenderse del lugar en el que están ubicadas y migrar a otros sitios a través de los sistemas venosos o linfáticos del individuo, hecho que conlleva a la aparición de nuevos tumores. La circunstancia antes descrita se conoce como metástasis (Lujambio & Lowe, 2012). Todas las células que hacen parte de un organismo vivo pueden llegar a convertirse en células cancerosas cuando la acumulación de mutaciones en algunos genes en particular conduce al deterioro de los mecanismos que controlan la proliferación celular (Inaki & Liu, 2012).
Desde principios del siglo veinte comenzaron a desarrollarse métodos terapéuticos para combatir el cáncer. La radioterapia y la quimioterapia, aproximaciones en las que se utilizan radiación y fármacos respectivamente, buscan eliminar las células tumorales; el efecto colateral del uso de estos tratamientos es el daño de células sanas y en algunos casos de todo el órgano en el que se encuentran (Martins, 2018; Galmarini, et al., 2012). Los dos tipos de tratamiento ocasionan en los pacientes pérdida de peso, vómito, caída del cabello, cefaleas permanentes y debilidad general entre otras. Una tercera alternativa terapéutica es la extirpación quirúrgica del tumor, sin embargo, uno de los riesgos de la intervención quirúrgica es que el procedimiento promueva eventos de metástasis (Alizadeh, et al., 2014).
Uno de los elementos fundamentales en la interacción entre el adenovirus oncolítico y la célula tumoral es la proteína fibra
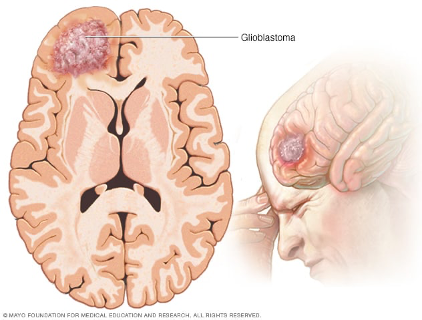
Imagen de: “Glioma” por la Clínica Mayo

Imagen de una resonancia magnética con un glioma en el hemisferio izquierdo por el Dr. José María Roda
En la década de los años noventa del siglo anterior se observó que pacientes con cáncer y que habían sufrido de infecciones virales mostraban algún grado de estabilización del crecimiento tumoral y en algunos casos remisión de la enfermedad (Wodarz, 2001). Los investigadores señalaron a los adenovirus humanos como responsables de las observaciones que habían hecho. A partir de 2016 se iniciaron algunas pruebas in vitro enfocadas en evaluar la capacidad de estos virus humanos para invadir y destruir de manera altamente selectiva las células tumorales (Witlox, et al., 2004).
Los adenovirus hacen parte de una familia de virus altamente contagiosos y que comúnmente atacan las mucosas de los sistemas respiratorio y nervioso, los ojos, los intestinos y las vías urinarias. Son los responsables de las epidemias anuales de bronquiolitis, conjuntivitis, pulmonía, meningitis y encefalitis (Scott, et al., 2016). En la mayoría de los casos las infecciones por adenovirus suelen ser bastante leves y por lo general el sistema inmunológico es capaz de eliminar los virus sin necesidad de un tratamiento médico complejo. Sin embargo, cuando la infección se presenta en bebes o adultos mayores con sistemas inmunes aún en desarrollo o inactivos, la enfermedad puede llegar a ser extremadamente severa. Este tipo de virus se caracteriza por presentar una cápside de forma icosaédrica y por ser el virus sin envoltura más grande, con un tamaño máximo que hace posible su transporte a través de los endosomas celulares (Nemerow, et al., 2012).
El adenovirus humano Ad5-Δ24-RGD ha sido utilizado en ensayos de laboratorio con el fin de evaluar su capacidad para destruir tumores de glioblastoma, un tipo de cáncer metastásico que ocurre en las células de soporte del tejido cerebral (Alemany, et al., 2000). Este es uno de los tumores más peligrosos debido a su ubicación y a lo rápido que puede llegar a generar efectos irreparables en el cerebro (Ohgaki & Kleihues, 2013). Este adenovirus ha probado ser sumamente valioso en los tratamientos experimentales contra el cáncer dado que se puede replicar durante semanas en el núcleo de la célula invadida, genera necrosis tumoral, desencadena una fuerte respuesta inmune y como consecuencia de todo lo anterior, a largo plazo induce la reducción del tamaño del tumor (Sato, et al., 2020).
En general, los virus oncolíticos funcionan como cualquier otro virus. Utilizan la maquinaria metabólica celular para multiplicar su material genético y también para producir nuevas partículas virales. Cuando las nuevas partículas virales han sido ensambladas, la célula invadida sufre citólisis y estas se liberan al medio externo. Finalmente, cada nuevo virus busca otra célula sana para invadirla y de esta manera reiniciar el ciclo infeccioso (Sewald, et al., 2016). A diferencia de lo descrito anteriormente, en los ensayos clínicos los virus oncolíticos son aplicados directamente en el tejido afectado mediante infiltración, viajan a través del torrente sanguíneo hasta llegar a la ubicación del tumor y proceden a invadir las células afectadas; en la medida en que se multiplican dentro de estas se reduce el tamaño del tumor y el sistema inmunológico es alertado sobre una amenaza para el cuerpo (Martínez-Vélez, et al., 2014).
A pesar de que se han hecho estudios clínicos que demuestran la capacidad del adenovirus Ad5-Δ24-RGD para invadir y destruir células cancerosas (Suzuki, et al., 2001; Fueyo, et al., 2003), no existen estudios que describan las variaciones en la configuración espacial de la proteína fibra portadora del péptido RGD-4C con respecto a la estructura de su homóloga nativa. La caracterización detallada de los cambios conformacionales que muestra la proteína fibra modificada es fundamental para comprender la relación que existe entre su configuración espacial y el incremento en la interacción de esta con las integrinas expresadas en la superficie de las células tumorales. En este trabajo se presenta una primera aproximación a la determinación de la estructura de la proteína fibra modificada del adenovirus Ad5-Δ24-RGD.

Proceso de infección de un virus oncolítico a una célula cancerígena por Laura Lerma
Materiales y métodos
Secuencias aminoacídicas de la proteína fibra
Las secuencias de las proteínas fibra nativa y modificada se obtuvieron de la base de datos Protein de NCBI. Los códigos de acceso son AAW65529 y AEB22086 respectivamente.
Alineamiento de las proteínas fibra nativa y modificada
Para determinar las diferencias existentes a nivel de secuencia primaria (secuencia aminoacídica) las dos proteínas se alinearon utilizando la herramienta BLAST (Basic Local Alignment Search Tool) de NCBI.
Modelaje por homología
El modelaje por homología para ambas proteínas se realizó utilizando el programa Swiss-Model (Waterhouse, et al., 2018), que cuenta con una base de datos de proteínas para las cuales ya existen modelos de estructura tridimensional. Swiss-Model compara la secuencia aminoacídica que se desea estudiar con la base de datos para identificar la proteína que sea más parecida y que tenga una estructura espacial previamente determinada.
Identificación de diferencias estructurales entre la proteína nativa y la proteína modificada
Las estructuras obtenidas en Swiss-Model fueron analizadas y modeladas con la aplicación Pymol para identificar los cambios estructurales ocurridos tras la inserción del motivo RGD (bucle HI) en la proteína modificada.

Unión del adenovirus a la célula por BQUB19 AAndorra (Wikipedia)
Resultados y discusión
El alineamiento de las dos proteínas (nativa y modificada) reveló que la primera tiene 581 aminoácidos mientras que la segunda tiene 590 puesto que presenta una inserción de nueve aminoácidos (CDCRGDCFC) en la posición 547 (figura 1). La comparación de las dos secuencias arrojó un grado de similitud de 98,47%, valor que se explica en función de la inserción anteriormente referida. El alineamiento mostró un valor E igual a cero (0), lo que indica que no hay probabilidad de que la proteína nativa muestre coincidencia con la proteína modificada por efecto del azar (Yu & Altschul, 2005).
Tras realizar el análisis de los modelos estructurales que mejor representaron a las secuencias primarias de las proteínas estudiadas, se seleccionaron los dos que mostraron los valores de similitud más altos con respecto a las configuraciones tridimensionales ya existentes para secuencias de aminoácidos semejantes. Para el caso de la proteína nativa se seleccionó el modelo que mostró una similitud del 100% y para la proteína modificada aquel con un nivel de similitud del 60%. El otro criterio que se consideró para la selección fue la cifra de QMEAN (Qualitative Model Energy Analysis), parámetro que opera como indicativo de la confiabilidad del modelo y cuyos valores pueden oscilar entre 0 y 1 (Benkert, et al., 2011). El modelo correspondiente a la proteína nativa obtuvo un QMEAN de 0,81, mientras que el de la proteína modificada mostró un valor de 0,73. Con base en los niveles de estos dos criterios se puede afirmar que los dos modelos son confiables.
La estructura de la proteína fibra nativa (modelo de cintas) reveló que la molécula es un trímero formado por monómeros de configuración similar (figura 2A); cada uno de ellos está constituido por once segmentos con estructura secundaria tipo hebra beta que están unidos entre sí por segmentos que muestran una estructura de tipo giro beta (figura 3). En la figura 2B se observa la aparición de 6 hebras beta (dos en cada monómero) como consecuencia de la inserción de los nueve aminoácidos del motivo RGD-4C (Branden, 1998). Tal como en el caso de la proteína trimérica nativa, las nuevas hebras beta que aparecen en los monómeros son antiparalelas y están conectadas a su correspondiente unidad por secciones que adoptan la configuración de giros beta (figura 4).

Figura 1. Comparación de las secuencias aminoacídicas de las proteínas fibra nativa y modificada de Ad5-Δ24-RGD. En cada bloque del alineamiento la primera línea corresponde a la proteína nativa y la tercera a la modificada.

Figura 2A. Estructura espacial (modelo de cintas) de la proteína fibra nativa de Ad5-Δ24 determinada con el programa Pymol.

Figura 2B. Estructura espacial (modelo de cintas) de la proteína fibra modificada de Ad5-Δ24-RGD determinada con el programa Pymol.
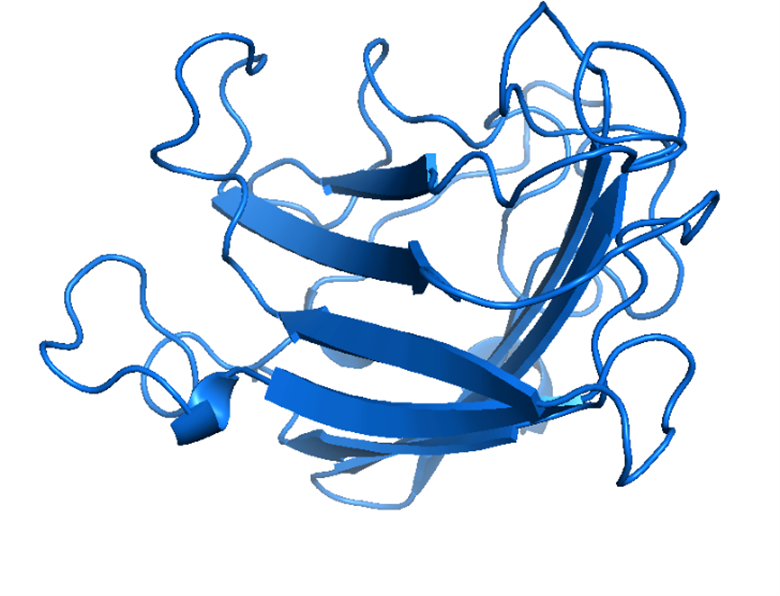
Figura 3. Estructura espacial (modelo de cintas) del monómero constitutivo de la proteína fibra nativa de Ad5-Δ24 determinada con el programa Pymol.

Figura 4. Estructura espacial (modelo de cintas) del monómero constitutivo de la proteína fibra modificada de Ad5-Δ24-RGD determinada con el programa Pymol.
La representación espacial de la proteína nativa (en modelo de superficie) evidenció una organización globular con un contorno relativamente homogéneo y un bolsillo en la parte central que corresponde a la región en la que se unen los tres monómeros que la constituyen (figura 5). De manera contrastante, la proteína modificada (figura 6) muestra cambios significativos en su contorno; aparecen tres protuberancias que corresponden a los motivos RGD-4C que fueron insertados tras la modificación del gen que codifica la proteína. La alteración de la superficie molecular se puede explicar en función de los impedimentos estéricos que se generan por cuenta de las configuraciones espaciales de las regiones insertadas (dos hebras beta por monómero) y las interacciones eléctricas que surgen tras la reorganización espacial de las regiones nuevas y las nativas (Branden, 1998). El bolsillo localizado en el centro de la molécula se mantuvo sin variaciones observables, lo que puede indicar que las inserciones y los efectos que estas provocan no afectan a las regiones centrales de cada monómero en las que se encuentran las hebras beta originales. La superposición de la proteína nativa sobre la proteína modificada (figura 7) evidencia las diferencias existentes entre las configuraciones espaciales de las dos moléculas. Las áreas opacas corresponden a las regiones en las que se localizan las protuberancias generadas por la inserción de los motivos RGD-4C.

Figura 5. Estructura espacial (modo superficie) de la proteína fibra nativa de Ad5-Δ24 determinada con el programa Pymol.

Figura 6. Estructura espacial (modo superficie) de la proteína fibra modificada de Ad5-Δ24-RGD determinada con el programa Pymol.
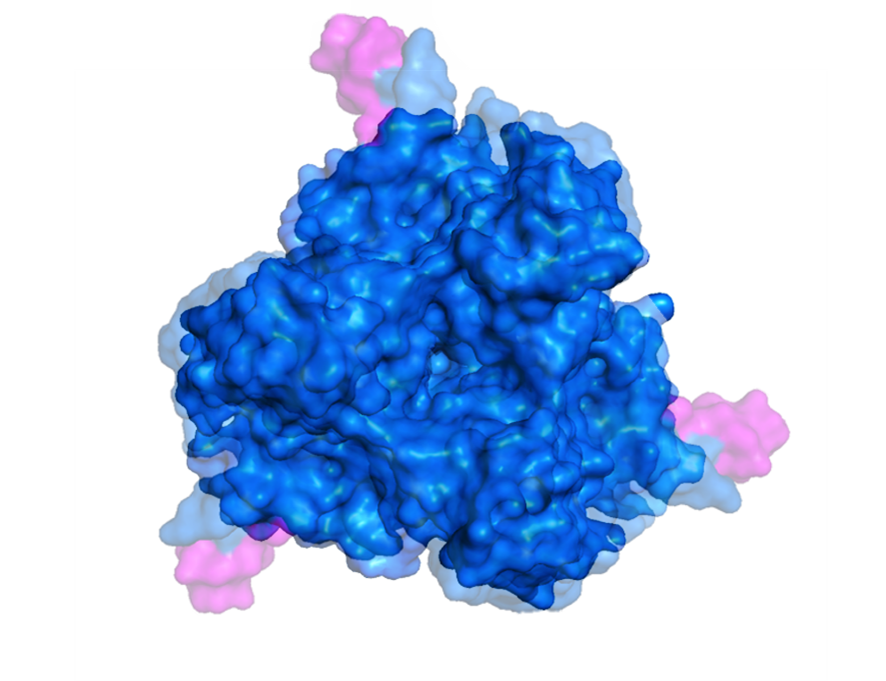
Figura 7. Superposición del modelo estructural (modo superficie) de la proteína fibra nativa sobre la proteína fibra modificada de Ad5-Δ24-RGD.
Conclusiones
La aproximación al modelo tridimensional de la proteína fibra modificada de Ad5-Δ24-RGD que se presenta en este estudio permitió determinar que la inserción del péptido RGD-4C provoca una significativa variación respecto a la estructura espacial de la proteína fibra nativa. El cambio referido implica la aparición de tres regiones (una por cada monómero) que adoptan una configuración de tipo hebra beta y que se manifiestan como protuberancias que provocan un cambio en el contorno de la proteína fibra como consecuencia de los impedimentos estéricos que están determinados por las interacciones eléctricas entre los aminoácidos localizados en los puntos de inserción del péptido RGD-4C (Branden, 1998).
Los trabajos de Suzuki et al. (2001) y Fueyo et al. (2003) ponen de manifiesto el aumento de la capacidad infectiva de Ad5-Δ24 a células tumorales derivado de la modificación de la porción distal de la proteína fibra con el péptido RGD-4C. Sin embargo, hasta el momento no se había propuesto ninguna explicación para el fenómeno. Witlox et al. (2004) demostraron que la presencia del motivo RGD en la proteína fibra es fundamental para que el virus logre interactuar con las integrinas de la superficie de la célula tumoral. Un mayor número de motivos RGD en el extremo de la proteína fibra de Ad5-Δ24-RGD puede explicar la notable variación en la capacidad infectiva observada en este virus oncolítico genéticamente modificado.
Lista de referencias
Alemany, R., Balague, C., & Curiel, D.T. (2000). Replicative adenoviruses for cancer therapy. Nat. Biotechnol.,18:723-7.
Alizadeh, A.M., Shiri, S., & Farsinejad, S. (2014). Metastasis review: from bench to bedside. Tumor Biol., 35: 8483-8523.
Benkert, P., Biasini, M., Schwede, T. (2011). Toward the estimation of the absolute quality of individual protein structure models. Bioinformatics (Oxford, England), 27 (3): 343-350.
Branden, C.I., & Tooze, J. (1998). Introduction to Protein Structure (2º ed.). Garland Science, New York. https://doi.org/10.1201/9781136969898
Fueyo, J., Alemany, R., Gómez‐Manzano, C., Fuller, G. N., Khan, A., Conrad, C. A., Liu, T., Jiang, H., Lemoine, M. G., Suzuki, K., Sawaya, R., Curiel, D.T., & Lang, F.F. (2003). Preclinical characterization of the antiglioma activity of a tropism‐enhanced adenovirus targeted to the retinoblastoma pathway. J. Natl. Cancer. Inst., 95: 652-60.
Galmarini, D., Galmarini, C. M., & Galmarini, F. C. (2012). Cancer chemotherapy: a critical analysis of its 60 years of history. Crit. Rev. Oncol. Hematol., 84 (2): 181-199.
Inaki, K., & Liu, E. T. (2012). Structural mutations in cancer: mechanistic and functional insights. Trends Genet., 28 (11): 550-559.
Jones, P. A., & Baylin, S. B. (2007). The epigenomics of cancer. Cell, 128 (4): 683-692.
Lujambio, A., & Lowe, S. (2012). The microcosmos of cancer. Nature, 482: 347-355.
Martínez-Vélez, N., Xipell, E., Jauregui, P., Zalacain, M., Marrodan, L., Zandueta, C., Vera, B., Urquiza, L., Sierrasesúmaga, L., Julián, M. S., Toledo, G., Fueyo, J., Gómez-Manzano, C., Torre, W., Lecanda, F., Patiño-García, A., & Alonso, M. M. (2014). The oncolytic adenovirus Δ24-RGD in combination with cisplatin exerts a potent anti-osteosarcoma activity. J. Bone Mine. Res., 29(10): 2287-2296.
Martins, P. N. (2018). A brief history about radiotherapy. Int. J. Lat. Res. Engin. Technol, 4 (2): 8-11.
Nemerow, G. R., Stewart, P. L., & Reddy, V. S. (2012). Structure of human adenovirus. Curr. Opin. Virol., 2 (2): 115-121.
Ohgaki, H., & Kleihues, P. 2013. The definition of primary and secondary glioblastoma. Clin. Cancer Res., 19 (4): 764-772.
Sato-Dahlman, M., LaRocca, C. J., Yanagiba, C., & Yamamoto, M. (2020). Adenovirus and immunotherapy: advancing cancer treatment by combination. Cancers, 12(5): 1295.
Scott, M. K., Chommanard, C., Lu, X., Appelgate, D., Grenz, L., Schneider, E., Gerber, S. I., Erdman, D. D., & Thomas, A. (2016). Human adenovirus associated with severe respiratory infection, Oregon, USA, 2013-2014. Emerg. Infect. Dis., 22(6): 1044-1051.
Sewald, X., Motamedi, N., & Mothes, W. (2016). Viruses exploit the tissue physiology of the host to spread in vivo. Curr. Opin. Cell Biol., 41:81-90.
Suzuki, K., Fueyo, J., Krasnykh, V., Reynolds, P. N., Curiel, D. T., & Alemany, R. (2001). A conditionally replicative adenovirus with enhanced infectivity shows improved oncolytic potency. Clin. Cancer Res., 7:120-126.
Waterhouse, A., Bertoni, M., Bienert, S., Studer, G., Tauriello, G., Gumienny, R., Heer, F. T., de Beer, T., Rempfer, C., Bordoli, L., Lepore, R., & Schwede, T. (2018). SWISS-MODEL: homology modelling of protein structures and complexes. Nucleic acids research, 46(W1), W296-W303.
Witlox, A. M., Van Beusechem, V. W., Molenaar, B., Bras, H., Schaap, G. R., Alemany, R., Curiel, D. T., Pinedo, H. M., Wuisman, P. I., & Gerritsen, W. R. (2004). Conditionally replicative adenovirus with tropism expanded towards integrins inhibits osteosarcoma tumor growth in vitro and in vivo. Clin. Cancer Res., 10(1): 61-7.
Wodarz, D. (2001). Viruses as antitumor weapons: defining conditions for tumor remission. Cancer Res., 61 (8): 3501-3507.
Yu, Y. K., & Altschul, S. F. (2005). The construction of amino acid substitution matrices for the comparison of proteins with non-standard compositions. Bioinformatics (Oxford, England), 21(7): 902-911.
